виды, свойства, способы удаления, применение, цена
Смесь оксидов железа, образовывающаяся при взаимодействии кислорода с раскалённым металлом, имеет обобщённое название — железная окалина. Она состоит из Fe3O4, FeO и Fe2O3 (магнетита, вьюстита и гематита соответственно) и представлена двумя легкоотделяемыми друг от друга слоями. При их суммарной толщине до 40 нм окалина невидима невооружённому взгляду, свыше 40 и до 500 нм — выдаёт себя цветами побежалости (радужным отливом). Постоянный же окрас появляется, если слой железной окалины на металле превышает 500 нм.

Состав
Наружный слой оксида железа — гематит. Он обладает большой твёрдостью (1030 ед. по шкале Виккерса), абразивностью и очень плохо растворяется в кислотах. Под ним в условиях частичной нехватки кислорода формируется более мягкий и почти нерастворимый в кислотах магнетит. Ближе всего к металлу находится рыхлый и мягкий вьюстит, который легко поддается устранению механическим путём или кислотным травлением.
Толщина каждого из трёх слоёв зависит от температуры обработки стали. Так, при превышении порога в 570 °C образуется чётко выраженная трёхслойная структура окалины. Дальнейшее повышение температуры ведёт к увеличению толщины вьюстита. Если же сталь обрабатывается при температурах ниже 570 °C, то в составе окалины преобладают магнетит и гематит.
По цвету железной окалины можно определить температуру обработки стали. Так, при температуре в 700–750 °C в составе окалины больше гематита, из-за чего она приобретает рыжевато-красный оттенок. Образовавшийся при высокотемпературном (900–1000 °C) прокате слой оксидов из-за более высокого процента вьюстита становится чёрным.
Особенности
Твёрдость окалины сочетается с её хрупкостью, из-за чего вкрапления оксида внутри структуры металла резко понижают его эксплуатационные характеристики. По этой же причине железная окалина не может быть использована в качестве защитного покрытия, хоть она и не взаимодействует с кислородом. Более того, в месте скола оксидов наблюдается усиленное окисление стали, что происходит из-за разности потенциалов окалины и стали. По этой причине её удаляют с готового проката.
Удаление окалины
Слой оксидов железа с прокатной стали удаляют со стальной заготовки несколькими способами.
Это очистка:
- механическая;
- химическая;
Возможно также сочетание вариантов.
Механическое воздействие на прокат сводится к пропуску проволоки или листа с окалиной через ряд роликов. При этом достигается частое изгибание заготовки, под воздействием которого железная окалина рассыпается на отдельные чешуйки и осыпается с металла. Для финишной очистки могут быть использованы абразивы, наждачные ленты, щётки из проволоки.
Достоинством этой технологии является сравнительная дешевизна и экологичность. Но поскольку отказ от смазки при такой обработке нецелесообразен, это приводит к замасливанию железной окалины, что затрудняет дальнейшую её переработку.
Химический и электрохимический способы очистки стали называют травлением. Для этих целей используются серная и соляная кислоты, реже — фосфорная, азотная, плавиковая или их смесь. Главными недостатками такого способа является одноразовое использование травильных растворов (не восстанавливаются) и низкий спрос на побочный продукт преобразования окалины — железный купорос. По этой причине травление применяется довольно редко, и ему обычно предшествует механическая очистка проката от окалины.
Применение окалины
Опытными кузнецами давно было примечено повышение сопротивляемости металла коррозии при формировании на нём тонкого слоя окалины. Сейчас же воронение оружейной стали используется лишь в качестве декоративной отделки. Её цвет зависит от способа обработки (кислота, щёлочь, температура) и толщины оксидной плёнки, составляющей от 1 до 10 мкм.

Прокатная окалина, удельный вес которой достигает 3% от общего веса готовых изделий, является ценным сырьём для металлургического производства за счёт высокого содержания (до 75%) в ней железа. Основное направление её переработки — очистка от примесей и восстановление, после которого она превращается в низкоуглеродистую сталь.
Некоторые составы окалины успешно применяются в качестве красящих пигментов и активно используются в строительстве. Также из окалины производится железный порошок, применяемый в металлургии, при изготовлении самонагревающихся смесей и даже в пищевой промышленности.
Химический состав этого отхода металлургической промышленности стандартизирован. Её стоимость может колебаться в зависимости от преобладания определённых видов окислов и количества примесей. Усреднённая цена на начало 2019 года составляла 50 американских долларов за тонну железной окалины.
Оцените статью:Рейтинг: 0/5 — 0 голосов
На поверхности изделий, получаемых путем горячей прокатки, присутствует железная окалина. Ее возникновение обусловлено особенностями данного производственного процесса. Окалина значительно сокращает коррозионную стойкость материала и усложняет последующую обработку, поэтому необходимо полное ее удаление.


Процесс образования
Рассматриваемое покрытие представлено продуктом окисления металла. Его формирование связано с высокими температурами и происходит при обработке металла температурой либо давлением. Прокат в любом случае покрыт окисным слоем. Он образуется на открытом воздухе в сухих условиях в виде пленок. Изначально они невидимы даже под микроскопом. Под термическим воздействием толщина окисного слоя возрастает до видимых размеров. Железной окалиной называют толстое покрытие, формирующееся при термическом воздействии в условиях открытого воздуха.
Состав формирующих его окисных соединений и структура определяется многими факторами: маркой стали, температурой, условиями среды, режимом термообработки, наличием и количеством окислителей.
Они представлены гематитом, магнетитом, вюститом. Первые два оксида железа характеризуются большой плотностью и соединены промежуточной структурой. Вюстит наоборот представлен пористым соединением. От названных выше оксидов он отличается большей диффузинной проницаемостью. Вюстит имеет с ними непрочную связь.


Структура железной оксидной пленки определяется окружающими условиями и температурой. Так, в кислородосодержащей среде при нагреве более 570 °C и быстром охлаждении формируется трехслойное покрытие. Внешний слой представлен гематитом, следующий – магнетитом и внутренний – вюститом. Как было отмечено, первые два имеют кристаллическую структуру и прочно взаимосвязаны. Внутренний слой пористой структуры непрочно контактирует с ними. Это обуславливает малое электросопротивление железной оксидной пленки и легкое ее отслаивание.
Для образования трехслойной окалины на металле необходимо соблюдение трех названных условий: высокой концентрации кислорода, температуры в 570 °C, быстрого ее снижения. Иначе формируется двух- или однослойная железная окалина.
Так, при меньшем нагреве слой вюстита получается тонким. В случае формирования железной окалины при высокой концентрации пара либо окислов углерода при малом количестве кислорода и температурах более 1000 °C гематит восстанавливается, вследствие чего отсутствует в составе. Таким образом, соотношение слоев напрямую определяется температурой. Так, при 700 °C толщина вюстита составляет 100 мкм, в то время как для магнетита и гематита – 10 и 1 мкм соответственно. Другими словами, состав железной окалины в значительной степени зависит от температуры. Так, при 700-900 °C она представлена почти на 90% вюститом, примерно на 10% магнетитом и менее чем на 1% гематитом. При большем нагреве и избытке кислорода происходит замещение вюстита гематитом.
В любом случае формирование слоев железной окалины происходит последовательно в соответствии с их расположением. При охлаждении вюстит утрачивает устойчивость и распадается до железа и гематита. Ввиду этого пленка обретает гематит-магнетитовый состав. При восстановлении гематит и магнетит переходят в железо и воду. Следовательно, в результате получается прокатная окалина, состоящая из железа.


Выше приведены основные закономерности и факторы возникновения железной окалины. В промышленных условиях процесс ее образования весьма сложен и может происходить неоднократно.
Методы удаления
Удаление окалины осуществляют тремя способами. Механический метод включает следующие варианты: пропускание материала через ряд роликов, обработку дробью и прочими абразивными материалами. Первая технология основана на деформации металла скручиванием, изгибом, растяжением. Такой способ позволяет убрать большую часть окалины. Его считают черновой обработкой, и после очищают материал дополнительно. Во втором случае осуществляют механическое воздействие на железную окалину металлической дробью, песком и прочими абразивными материалами. Наконец, существуют механизированные технологии, связанные с применением микрорезцовых инструментов, проволочных щеток, наждачных лент и т. д.
Химические методы подразумевают обработку деталей в кислотах, солях, щелочах, называемую травлением. При этом большое значение имеет растворимость составляющих железную окалину соединений в кислотах. Так, вюстит легко подвержен ему, в отличие от магнетита. Гематит считают нерастворимым. Травление дифференцируют на химическое и электрохимическое. Далее рассмотрены некоторые варианты.
Травление серной кислотой связано с образованием водорода и проникновением его в металл, что ведет к водородной хрупкости, снижающей механические параметры и затрудняющей последующую обработку материала. Поэтому с целью сокращения наводораживания приходится долго выдерживать металл по завершении травления либо нагревать при сушке. К тому же во избежание разрушения металла кислотой после растворения железной окалины используют ингибиторы. Нужно отметить, что в нагретом растворе сталь разрушается быстрее.
Травление соляной кислотой идет по тем же закономерностям. Однако, в отличие от серной, для этого не требуется нагрев. Напротив, при температуре более 40°C выделяются хлороводородные соединения. В процессе травления формируются хлористые соли железа. В целом обработка соляной кислотой, в сравнении с серной, обеспечивает лучшую очистку при меньшем наводораживании стали.
Электрохимический способ существенно повышает скорость очистки металла от окалины и сокращает водородную хрупкость, а также расход раствора. Его дифференцируют на анодный, катодный и смешанный варианты.
Выбор способа очистки определяется многими факторами, среди которых состав изделия, целевые параметры, последующая обработка и т. д.
Окалина — это… Что такое Окалина?
 Искры, летящие от стали при шлифовке, состоят из железной окалины
Искры, летящие от стали при шлифовке, состоят из железной окалиныОкалина — это смесь оксидов, образующихся прямым действием кислорода при накаливании на воздухе металлов. Обычно термин применяется к оксидам не всех металлов, а только железа и меди.
Железная окалина представляет собой смесь оксидов Fe3O4, FeO и Fe2O3, и состоит из двух слоев, легко отделяемых друг от друга. Внутренний слой пористый, черно-серого цвета, наружный плотный и с красноватым оттенком, оба слоя хрупки и обладают ферромагнитными свойствами. Состав железной окалины непостоянен и зависит от условий получения: при продолжительном накаливании на воздухе она постепенно переходит в Fe2O3, а последняя в белокалильном жару теряет часть кислорода, переходя в FeO. Обычно железная окалина состоит из 64-73% FeO и 36-27% Fe
Медная окалина, представляющая собой хрупкую, черно-серого цвета массу, состоит из оксидов меди Cu2O (около 75 %) CuO (около 25 %). Так же как у железной окалины, состав её непостоянен и может колебаться в зависимость от температуры и избытка кислорода при получении. Во внутренних слоях преобладает Cu
Применение
- Окалина содержит до 75 % металла и является ценным сырьём в металлургическом производстве.
- Медная окалина используется при очистке медных сплавов от алюминия.
- Преднамеренное покрытие стальных и чугунных изделий тонким слоем (1-10 мкм) железной окалины — воронение — применяется в декоративных целях.
Цена
На больших металлургических предприятиях железная окалина является многотоннажным побочным продуктом. Содержит до 75% железа. Её состав стандартизован (например «Окалина прокатного производства ГОСТ 27А 2787-75») и продаётся по цене ~50 $/т [1]
См. также
Литература
Ссылки
Виды и типы железной окалины
Железная окалина представляет собой продукт окисления металла. Образование железной окалины связанно с процессами термической обработки или обработки металла давлением при высоких температурах..
На поверхности стального проката всегда присутствует окисный слой. Состав и структура окисных соединений будет зависеть от марки стали, состава окружающей среды, температуры, режима термообработки, наличия и количества окислителей, например кислорода и ряда других факторов.
В сухой воздушной среде при низких температурах возникают очень тонкие окисные пленки, которые невозможно увидеть даже при увеличении поверхности металла под микроскопом. При увеличении температуры толщина окисного слоя увеличивается, и получаются хорошо различимые окисные слои.
При производстве проката поверхность металла часто подвергается высокотемпературному воздействию в присутствии кислорода воздуха, что приводит к образованию толстого многослойного окисного слоя, называемого окалиной.
При окислении образуются разные оксиды железа, такие как FeO (вюстит), Fe
4FeO=Fe3O4+Fe.
Поэтому, в данном случае оксидная пленка, практически состоит из магнетита и гематита.
Восстановление полученной оксидной пленки происходит по реакциям:
Fe3O4+4H2=3Fe+4H2O; Fe2O3+3H2=2Fe+3H2O.
Восстановленный слой состоит из практически чистого железа.
Зависимость скорости превращения окислов от температуры представлена на рисунке 1.
Рисунок 1- Зависимость скорости превращения окислов от температуры
Строение окалины на поверхности проката в основном соответствует правилу последовательности превращений. Сначала к металлу примыкает вюстит, затем магнетит, и затем внешний слой — гематит. Вюстит легко растворим в минеральных кислотах, в отличие от магнетита и гематита. Магнетит в меньшей степени растворяется в кислотах. Гематит же считается нерастворимым соединением.
Трехслойное образование железной окалины получается только при температуре свыше 570оС и при высоком содержании кислорода, а также при быстром охлаждении. В других условиях образуется двухслойная или однослойная железная окалина. Если окисление железа проходит при температуре меньше 570оС, то слой вюстита образуется в виде очень тонкой пленки под слоем окалины, которая состоит из магнетита и гематита. Чем ниже температура, тем тоньше слой вюстита. Если процесс окисления происходит при температуре 700оС, то толщина слоя вюстита будет 100 мкм, слоя магнетита 10 мкм, а гематита — 1 мкм. Если окалина образуется при низком содержании кислорода и высоком содержании водяного пара или окислов углерода, особенно при температуре свыше 1000оС, то в составе окалины не обнаруживают гематита, так как он восстанавливается.
Окалина железа, образующаяся на поверхности проката представляет собой смесь различных фаз, причем состав окалины и ее структура будут определяться режимом тепловой обработки металла. Обычно образуется трехслойная окалина железа, при этом доля каждого окисного соединения в окалине будет зависеть от температуры окисления. При температуре 700-900оС окалина железа состоит из 10% магнетита и 90% вюстита, а при увеличении температуры свыше 900оС и при появлении избытка кислорода вместо вюстита начинает возникать слой гематита.
Структура железной окалины, получающейся в промышленных условиях всегда более сложная. Это связанно с влиянием различных легирующих элементов, находящихся в стали, неравномерностью состава стали и особенностями производства металла.
Например, условия, определяющие образование прокатной окалины на горячекатаном прокате, зависят также и от режима работы стана горячей прокатки. Перед чистовой группой клетей окалина удаляется водой. Но, при прохождении металла через чистовую группу клетей, и в процессе охлаждения металла, прокатная окалина образуется вновь. И, в зависимости от условий прохождения металла, существует несколько различных типов окалины на горячекатаном металле.
Рекомендуем ознакомиться со статьями:
- Окалина железа на горячекатаной полосе металла
- Влияние температуры и условий охлаждения на формирование железной окалины
- Немного об окалине
- Дефект металла «Раковины от окалины»
- Травление металла
Окалина — Википедия. Что такое Окалина
Материал из Википедии — свободной энциклопедии Искры, летящие от стали при шлифовке, состоят из железной окалины
Искры, летящие от стали при шлифовке, состоят из железной окалиныОка́лина — это смесь оксидов, образующихся прямым действием кислорода при накаливании на воздухе металлов. Обычно термин применяется к окислам не всех металлов, а только железа и меди.
Железная окалина представляет собой смесь оксидов Fe3O4, FeO и Fe2O3, и состоит из двух слоев, легко отделяемых друг от друга. Внутренний слой пористый, черно-серого цвета, наружный плотный и с красноватым оттенком, оба слоя хрупки и обладают ферромагнитными свойствами. Состав железной окалины непостоянен и зависит от условий получения: при продолжительном накаливании на воздухе она постепенно переходит в Fe2O3, а последняя в белокалильном жару теряет часть кислорода, переходя в FeO. Обычно железная окалина состоит из 64—73 % FeO и 36—27 % Fe2O3, наружный слой содержит больше Fe2O3 — от 32 до 37 %, а самый внешний слой даже до 53 %. На поверхности легированных сталей образуются сложные оксиды (NiO·Fe2O3, FeO·Cr2О3 и др.). При толщине до 40 нм слой окалины прозрачный, при толщине от 40 до 500 нм — окрашен в тот или иной цвет побежалости, при толщине свыше 500 нм окалина имеет постоянную окраску, зависящую от химического состава.
Медная окалина, представляющая собой хрупкую, чёрно-серого цвета массу, состоит из окислов меди Cu2O (около 75 %) CuO (около 25 %). Так же как у железной окалины, состав её непостоянен и может колебаться в зависимости от температуры и избытка кислорода при получении. Во внутренних слоях преобладает Cu2O, в наружных — CuO. При красном калении и при достаточном количестве кислорода Cu2O окисляется до CuO, поэтому в этих условиях медная окалина будет состоять главным образом из CuO, а при температурах выше 1100 °С, вследствие разложения CuO на Cu2O и кислород, в медной окалине будет преобладать Cu2O.
Применение
- Окалина содержит до 75 % металла и является ценным сырьём в металлургическом производстве.
- Медная окалина используется при очистке медных сплавов от алюминия.
- Преднамеренное покрытие стальных и чугунных изделий тонким слоем (1—10 мкм) железной окалины — воронение — применяется в декоративных целях.
Цена
На больших металлургических предприятиях железная окалина является многотоннажным побочным продуктом. Содержит до 75 % железа. Её состав стандартизован (например, «Окалина прокатного производства ГОСТ 27А 2787-75[1]») и продаётся по цене ~50 $/т[2].
См. также
Литература
Ссылки
В силу ряда особенностей горячей прокатки и последующего охлаждения горячекатаных полос их поверхность покрыта окалиной неодинаковой толщины и различного фазового состава. В результате взаимодействия железа с кислородом среды, в которой оно находится при сравнительно высоких температурах, образуются три устойчивых окисла: вюстит (FeO), магнетит (Fe3O4) и гематит (Fe2O3). Слои, составляющие окалину, располагаются таким образом, что непосредственно к металлу примыкает слой окисла с наименьшим содержанием кислорода FeO, далее следует средний слой промежуточного состава Fe3O4, наружный слой окалины состоит из высшего окисла Fe2O3. Соотношение толщин слоев и одновременное существование всех трех окислов зависят от условий окисления поверхности железа.
Важная характеристика окалины – ее сплошность (пористость). Трещины и поры возникают в слое окалины в период охлаждения металла в результате преобразований структуры. При образовании окалины, состоящей из вюстита, приращение объема составляет 1,76 , а из магнетита и гематита соответственно 2,1 и 2,4. Чем выше температура окисления, тем больше образуется различных окислов, обладающих разной пластичностью. Превращение их приводит к возникновению внутренних напряжений, вызывающих образование трещин и пор. При травлении в соляной кислоте быстрее всего растворяется закись железа (вюстит), образующий наиболее пористый слой. Однако вюстит обычно содержится только в слое окалины, прилегающем к металлу. Наружный слой состоит из магнетита и гематита, которые растворяются незначительно. Наличие пор и трещин в окалине ускоряет травление. Раствор кислоты проникает через эти несплошности к поверхности металла и слою вюстита. Наряду с растворением вюстита происходит взаимодействие ионов водорода кислоты с металлическим железом. По мере растворения слоя вюстита уменьшается прочность сцепления окалины с основным металлом. Выделяющийся водород восстанавливает высшие окислы железа до закиси. Процесс растворения окалины, не содержащей вюстита, протекает медленнее и связан с повышенными потерями металла.
Опыт работы травильных линий показывает, что продолжительность травления окалины в значительной степени связана с температурой смотки, которая влияет на толщину и структуру окалины. Обычно сокращение продолжительности травления с уменьшением температуры смотки связывают со снижением степени превращения вюстита (FeO) в магнетит (Fe3O4), а также с уменьшением опасности появления гематита (Fe2O3) по кромкам полосы. При этом предполагается, что удаление окалины происходит путем растворения вюститной фазы вдоль границы раздела сталь-окалина и подвода кислоты к границе металла. При взаимодействии кислоты с железом образуется водород, который способствует отслоению окалины. При высокой температуре смотки на границе раздела фаз окалина-сталь вюстит отсутствует, т.е. основным механизмом удаления окалины является на отслоение гематита и магнетита, а их растворение.
С целью выяснения механизма влияния температуры смотки на продолжительность травления изучали фазовый состав окалины. Образцы железной окалины были отобраны от головной, средней и хвостовой частей полос, температура смотки которых составляла 580-600, 640-680 и 700-730 0С. Изучение окалины проводили комплексными методами. На начальных этапах использовали химические методы селективного изолирования фаз. Общий состав оксидных фаз изолировали методом галогенирования в атмосфере сухого газообразного хлора при температуре 3500С. После удаления хлора путем вымораживания смесь оксидов и хлоридов нагревали до температуры возгонки. После возгонки FeCl2 оксидные фазы переводили в раствор путем сплавления с персульфатом калия и количественный анализ по составляющим элементам вели химическим и атомно-абсорбционными методами на спектрофотометре.
Таблица 1 – Фазовый состав железной окалины при различной температуре смотки полос
Температура смотки, 0С | Фазовые составляющие *, % | |||||
SiO2 | Al2O3 | Fe3O4 | FeO | Fe2O3 | Fe (метал.) | |
580-600 | 1,29 2,31 1,51 | 0,69 0,71 0,93 | 52,62 47,13 52,65 | — 0,73 1,23 | — — — | 45,40 49,12 43,63 |
640-680 | 1,56 2,49 1,83 | 1,31 1,14 1,17 | 63,96 53,04 53,53 | — 7,21 11,36 | — — — | 33,17 36,12 32,11 |
700-730 | 2,30 1,85 1,60 | 1,02 1,02 1,00 | 61,88 47,17 33,05 | 8,26 43,14 45,95 | 10,58 8,31 — | 16,07 17,31 18,40 |
* — Верхнее, среднее и нижнее значения содержания фаз в каждом диапазоне температур соответствуют головной, средней и хвостовой частям полосы при горячей прокатке | ||||||
Результаты исследований показывают, что количество оксидов кремния, алюминия и магния существенно не изменяются в окалине, полученной при различных температурах смотки.
Дополнительно для определения оксидных фаз железа в окалине использовали метод ядерной гамма-резонансной спектроскопии (ЯГР). Спектры снимали с образцов окалины без дополнительных физико-химических обработок. Было установлено, что характер кривых спектров, снятых с образцов окалины, полученной при низкой и высокой температурах смотки, в основном аналогичен. Основной фазой в окалине на металле головной части полосы при низкой температуре смотки является гематит. При высокой температуре смотки в окалине головной части полосы также основной фазой является гематит с небольшой примесью вюстита и гематита (последний, очевидно, появляется за счет дополнительного окалинообразования при охлаждении рулонов с повышенной температурой). Окалина средней части полосы при низкой температуре смотки характеризуется преимущественно магнетитной фазой. Для хвостовых частей полос при низкой и высокой температурах смотки соотношение фаз магнетита и вюстита в окалине колеблется от 1:1 до 1:0,7. Общее количество оксидных фаз в окалине при увеличении температуры смотки с 580-620 до 700-7300С возрастает в среднем в 1,5 раза. Наибольшее количество железа в окалине (43-49%) приходится на полосу с температурой смотки 580-6200С. С увеличением температуры смотки до 700-7300С количество металлического железа в окалине снижается до 16-18%. Количественное соотношение оксидных фаз и металлического железа в окалине, взятой с краев полосы при низкой и высокой температурах смотки, такое же, что и в средней части полосы.
Основной фазой в металлической окалине стали 08Ю может быть не только магнетит, но и вюстит, как при низкой так и при высокой температуре смотки. Гематит в окалине присутствует лишь при высокой температуре смотки. С понижением температуры смотки общее количество труднорастворимых оксидов (гематита и магнетита) изменяется незначительно, а количество легкорастворимой закиси железа (вюстит) уменьшается. Следовательно, изменение содержания оксидных фаз и их соотношения не могут объяснить увеличение скорости травления металла с понижением температуры смотки. Фактором, объясняющим повышение интенсивности травления металла, является содержание металлического железа, которое увеличивается обратно пропорционально температуре смотки полосы.
Некоторые дефекты металла, связанные с окалиной (фото, описание и как бороться):
Плюс к этому Краткий отчет исследования выкатываемости окалины (Трансформация дефекта «Окалина»)
А также важно понимать для чего необходим ингибитор травления.
В завершение короткое прикольное видео Непрерывно-травильный агрегат для удаления окалины:
Рекомендуем ознакомиться со статьями:
- Окалина железа на горячекатаной полосе металла
- Механизм образования железной окалины на поверхности стали
- Травление металла
- Влияние температуры и условий охлаждения на формирование железной окалины
- Окалина, дефекты травления металла и зачем нужен ингибитор
Железная окалина
Железная окалина цена от 300руб/кг
(окалина прокатного производства при производстве арматуры, металлическая окалина, смесь окислов железа)
Минимальная партия на продажу от 1кг
Химический состав окалины: Железо -92,8% Углерод -менее 0,015% Кремний-0,05% Марганец-0,55% Хром-0,08% Медь-0,36% Ванадий-0,06%
Сертификат с химсоставом выложен ниже
Размер кусков: от 0,1 до 1,5см
Формула: смесь оксидов железа Fe2O3, Fe3O4, FeO
Производство Россия
В случае необходимости бесплатно предоставим образцы 10гр
Быстрая доставка по Москве и регионам
Всегда в наличии на складе
Видео и фотография как выглядит металлическая окалина
| Железная окалина |
 |
| Видео как выглядит железная окалина |
|
| Химический состав железной окалины |
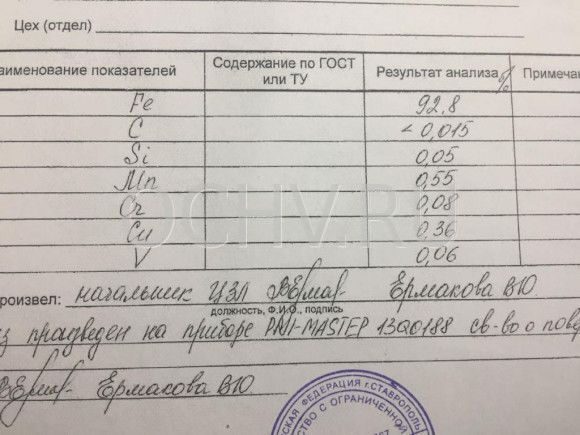 |
| Окалина |
 |
Условия и способ оплаты
Условия и способ доставки
Гарантия на товар
Возврат и обмен
Оставить отзыв о товаре
Акции, скидки, распродажа
Отправить заявку или заказать обратный звонок
Купить товар можно по номеру телефона: (495) 923-81-68 или [email protected]
Сертификаты
Специалисты компании
Справочник
Схема проезда
Смотрите также другие виды железа:порошок, карбонильное радиотехническое Р-10, сплавы железа, окалина, карбонильное осч 6-2, карбонильное осч 13-2, сернистое Ч, окись Ч, сернокислое окисное ч, нано оксид железа,
Что такое оксид железа? (с картинками)
Оксид железа — это любое из ряда химических соединений, состоящих из железа и кислорода. Большинство из них встречаются в природе; некоторые формы в почве или в химических отложениях в скалах или горах, и ржавчина также является очень распространенным и известным источником. Не все оксиды полезны для человека, но несколько разновидностей играют ключевую роль в промышленности, косметике и искусстве. Производители часто полагаются на них для добавления пигмента, а также для придания определенных электронных и магнитных свойств таким вещам, как банковские карты и устройства цифрового сканирования.
 Оксид железа ржавчина на поверхности цепи.
Оксид железа ржавчина на поверхности цепи.Откуда
Железо представляет собой металлический элемент с химическим символом Fe и является одним из самых плодовитых и распространенных минеральных веществ на Земле.По оценкам ученых, оно находится примерно в 5% земной коры и также существует в ее ядре. Железо превращается в оксид железа, когда вступает в контакт с кислородом, либо самостоятельно, либо в сочетании с другими элементами, такими как вода. Когда минерал подвергается воздействию воды и воздуха в течение длительных периодов времени, он обычно производит ржавчину, которая представляет собой красновато-коричневый оксид.
 Черный железоокисный пигмент часто используется в тушь и другую косметику.
Черный железоокисный пигмент часто используется в тушь и другую косметику.Хотите автоматически сэкономить время и деньги месяца? Пройдите 2-минутный тест, чтобы узнать, как начать экономить до 257 долларов в месяц.
Отложения оксида железа встречаются и в почве. Эксперты, как правило, полагают, что они были созданы в результате осаждения железа из морской воды во время протерозоя около 1 года.6 миллиардов лет назад. Эти месторождения находятся в разных точках мира, хотя наибольшая концентрация наблюдается в Соединенных Штатах, Индии, Австралии, Китае, Бразилии и России.
 Некоторые солнцезащитные средства изготавливаются с использованием оксида железа.
Некоторые солнцезащитные средства изготавливаются с использованием оксида железа.разных типов
Железо окисляется несколькими различными путями, и результаты попадают в разные области спектра: одни в основном железо, а другие — кислород.Конечный цвет и технические характеристики варьируются соответственно. Существуют две первичные формы, известные как (II) и (III), оксида в природе, хотя различные элементы и соединения иногда получают из обоих источников. Например, ржавчина известна как оксид железа (II, III) и имеет химическую структуру Fe 2 O 3 , хотя обозначение (II, III) равно и дано магнетиту, соединению со структурой Fe 3 O 4 ; ряд других соединений также может быть включен в эту группу.В большинстве случаев числовые обозначения говорят больше о том, как элементарное железо и кислород связываются вместе, чем то, на что похоже вещество.
 Оксид железа можно найти в лаке для обуви.
Оксид железа можно найти в лаке для обуви.Цвет тоже имеет значение.В большинстве случаев железо с высокими концентрациями (II) имеет тенденцию к глубокому черному и угольному цвету, тогда как железо с (III) составом больше падает на красновато-коричневый конец спектра. Например, планету Марс часто называют «красной планетой» благодаря высокой концентрации оксида железа (III) в ее коре и почве.
 Оксид железа можно найти в тени для век.
Оксид железа можно найти в тени для век.Использование в электронике
Среди стабильных элементов с комнатной температурой обычно есть только три, которые являются естественно магнитными, а именно кобальт, никель и железо; среди них железо обычно является наиболее магнитным, что производители часто используют при производстве магнитов, электронных компонентов, аудио- и видеокассет, а также банковских и намагниченных кредитных карт.В этих случаях немного порошкообразного оксида объединяется с другими элементами и герметиками для создания магнитных лент или лент, которые можно использовать, чтобы помочь держать рабочие части заряженными и на месте. То, что оксид встречается в природе естественным образом, также помогает снизить затраты.
 Пигментация, использованная в наскальных рисунках в Ласко, была получена из оксида железа.
Пигментация, использованная в наскальных рисунках в Ласко, была получена из оксида железа.Косметические аппликации
Косметическая промышленность использует состав для создания различных пигментов в косметике.Большинство оксидных форм нетоксичны, водоотталкивающие, не текут и не кровоточат, что делает их идеальной добавкой к таким продуктам, как тушь, жидкая и порошковая основа и тени для век. Оксиды также можно найти в некоторых типах продуктов для здоровья, таких как тальк, крем для лица и крем для тела. Некоторые солнцезащитные средства также содержат его. Считается, что его структура помогает блокировать вредные ультрафиолетовые лучи солнца от повреждения кожи человека.
Важность в искусстве
В мире искусства оксид железа используется для создания пигментов, таких как жженая сиена и жженая янтарь.Цвета и краски, изготовленные таким образом, имеют тенденцию быть постоянными и долговечными. Хотя точный метод окрашивания красок несколько изменился с течением времени, основная концепция играла с доисторического периода; Наскальные рисунки в Ласко, Франция, являются лишь одним из примеров того, как долго этот состав использовался и как долго сохраняются краски, сделанные с помощью железа. Современные производители редко используют только для формирования базовых цветов и пигментных основ, хотя он часто остается важным компонентом.
в промышленности
Компаунд в его различных типах и комбинациях находит широкое применение в промышленности. Пигменты часто используются для окрашивания таких вещей, как, например, краска промышленного качества, бетон, кожа и крем для обуви; такие продукты, как плитка и резина, иногда также содержат его для цвета и стабильности.Оксид железа также добавляют в различные питательные вещества, корма и лекарства в следовых количествах, обычно в качестве способа поддержания химического баланса между различными активными ингредиентами.
 Оксид железа можно найти в креме для лица. ,
Оксид железа можно найти в креме для лица. ,% PDF-1.5 % 24 0 объектов> endobj Xref 24 813 0000000016 00000 n 0000017819 00000 n 0000017956 00000 n 0000016888 00000 n 0000018036 00000 n 0000018215 00000 n 0000035868 00000 n 0000035944 00000 n 0000035978 00000 n 0000036020 00000 n 0000049230 00000 n 0000064766 00000 n 0000079776 00000 n 0000094030 00000 n 0000107088 00000 n 0000120039 00000 n 0000120294 00000 n 0000120554 00000 n 0000120811 00000 n 0000121073 00000 n 0000121318 00000 n 0000121557 00000 n 0000121993 00000 n 0000122386 00000 n 0000122858 00000 n 0000123260 00000 n 0000123731 00000 n 0000124276 00000 n 0000135559 00000 n 0000150290 00000 n 0000164483 00000 n 0000186380 00000 n 0000197741 00000 n 0000200410 00000 n 0000200462 00000 n 0000200636 00000 n 0000200800 00000 n 0000200964 00000 n 0000201138 00000 n 0000201306 00000 n 0000201477 00000 n 0000201645 00000 n 0000201810 00000 n 0000201981 00000 n 0000202149 00000 n 0000202314 00000 n 0000202485 00000 n 0000202653 00000 n 0000202824 00000 n 0000202992 00000 n 0000203163 00000 n 0000203331 00000 n 0000203502 00000 n 0000203673 00000 n 0000203838 00000 n 0000204003 00000 n 0000204171 00000 n 0000204339 00000 n 0000204504 00000 n 0000204672 00000 n 0000204840 00000 n 0000205005 00000 n 0000205176 00000 n 0000205344 00000 n 0000205509 00000 n 0000205680 00000 n 0000205848 00000 n 0000206016 00000 n 0000206182 00000 n 0000206350 00000 n 0000206518 00000 n 0000206686 00000 n 0000206854 00000 n 0000207020 00000 n 0000207188 00000 n 0000207356 00000 n 0000207521 00000 n 0000207690 00000 n 0000207856 00000 n 0000208022 00000 n 0000208191 00000 n 0000208357 00000 n 0000208522 00000 n 0000208688 00000 n 0000208854 00000 n 0000209020 00000 n 0000209186 00000 n 0000209352 00000 n 0000209521 00000 n 0000209687 00000 n 0000209856 00000 n 0000210022 00000 n 0000210191 00000 n 0000210360 00000 n 0000210526 00000 n 0000210692 00000 n 0000210861 00000 n 0000211027 00000 n 0000211196 00000 n 0000211362 00000 n 0000211528 00000 n 0000211694 00000 n 0000211859 00000 n 0000212003 00000 n 0000212168 00000 n 0000212302 00000 n 0000212468 00000 n 0000212634 00000 n 0000212803 00000 n 0000212969 00000 n 0000213135 00000 n 0000213301 00000 n 0000213467 00000 n 0000213604 00000 n 0000213770 00000 n 0000213936 00000 n 0000214105 00000 n 0000214272 00000 n 0000214441 00000 n 0000214578 00000 n 0000214745 00000 n 0000214914 00000 n 0000215080 00000 n 0000215221 00000 n 0000215387 00000 n 0000215553 00000 n 0000215722 00000 n 0000215859 00000 n 0000216025 00000 n 0000216166 00000 n 0000216307 00000 n 0000216473 00000 n 0000216614 00000 n 0000216780 00000 n 0000216946 00000 n 0000217112 00000 n 0000217249 00000 n 0000217386 00000 n 0000217527 00000 n 0000217668 00000 n 0000217805 00000 n 0000217942 00000 n 0000218083 00000 n 0000218252 00000 n 0000218389 00000 n 0000218526 00000 n 0000218663 00000 n 0000218804 00000 n 0000218945 00000 n 0000219082 00000 n 0000219223 00000 n 0000219364 00000 n 0000219530 00000 n 0000219671 00000 n 0000219808 00000 n 0000219945 00000 n 0000220082 00000 n 0000220223 00000 n 0000220364 00000 n 0000220501 00000 n 0000220638 00000 n 0000220779 00000 n 0000220920 00000 n 0000221061 00000 n 0000221202 00000 n 0000221343 00000 n 0000221480 00000 n 0000221621 00000 n 0000221762 00000 n 0000221903 00000 n 0000222044 00000 n 0000222185 00000 n 0000222326 00000 n 0000222467 00000 n 0000222608 00000 n 0000222749 00000 n 0000222886 00000 n 0000223027 00000 n 0000223168 00000 n 0000223309 00000 n 0000223450 00000 n 0000223616 00000 n 0000223757 00000 n 0000223894 00000 n 0000224031 00000 n 0000224172 00000 n 0000224313 00000 n 0000224454 00000 n 0000224623 00000 n 0000224789 00000 n 0000224930 00000 n 0000225071 00000 n 0000225237 00000 n 0000225378 00000 n 0000225519 00000 n 0000225685 00000 n 0000225826 00000 n 0000225967 00000 n 0000226108 00000 n 0000226249 00000 n 0000226390 00000 n 0000226556 00000 n 0000226693 00000 n 0000226859 00000 n 0000226996 00000 n 0000227137 00000 n 0000227303 00000 n 0000227440 00000 n 0000227581 00000 n 0000227750 00000 n 0000227891 00000 n 0000228032 00000 n 0000228173 00000 n 0000228310 00000 n 0000228479 00000 n 0000228616 00000 n 0000228757 00000 n 0000228894 00000 n 0000229031 00000 n 0000229172 00000 n 0000229313 00000 n 0000229450 00000 n 0000229617 00000 n 0000229758 00000 n 0000229899 00000 n 0000230036 00000 n 0000230177 00000 n 0000230318 00000 n 0000230484 00000 n 0000230653 00000 n 0000230794 00000 n 0000230931 00000 n 0000231072 00000 n 0000231209 00000 n 0000231375 00000 n 0000231512 00000 n 0000231649 00000 n 0000231818 00000 n 0000231955 00000 n 0000232096 00000 n 0000232233 00000 n 0000232374 00000 n 0000232515 00000 n 0000232652 00000 n 0000232818 00000 n 0000232955 00000 n 0000233121 00000 n 0000233258 00000 n 0000233427 00000 n 0000233593 00000 n 0000233730 00000 n 0000233871 00000 n 0000234037 00000 n 0000234178 00000 n 0000234319 00000 n 0000234460 00000 n 0000234601 00000 n 0000234742 00000 n 0000234883 00000 n 0000235024 00000 n 0000235161 00000 n 0000235298 00000 n 0000235439 00000 n 0000235580 00000 n 0000235721 00000 n 0000235862 00000 n 0000236003 00000 n 0000236144 00000 n 0000236313 00000 n 0000236450 00000 n 0000236616 00000 n 0000236753 00000 n 0000236922 00000 n 0000237088 00000 n 0000237254 00000 n 0000237422 00000 n 0000237592 00000 n 0000237760 00000 n 0000237928 00000 n 0000238094 00000 n 0000238825 00000 n 0000238991 00000 n 0000239722 00000 n 0000239888 00000 n 0000240054 00000 n 0000240785 00000 n 0000240951 00000 n 0000241682 00000 n 0000241848 00000 n 0000242014 00000 n 0000242180 00000 n 0000242352 00000 n 0000242518 00000 n 0000242684 00000 n 0000242850 00000 n 0000243022 00000 n 0000243188 00000 n 0000243360 00000 n 0000243532 00000 n 0000243704 00000 n 0000243876 00000 n 0000244042 00000 n 0000244214 00000 n 0000244386 00000 n 0000244558 00000 n 0000244730 00000 n 0000244902 00000 n 0000245074 00000 n 0000245240 00000 n 0000245412 00000 n 0000245584 00000 n 0000245756 00000 n 0000245928 00000 n 0000246100 00000 n 0000246272 00000 n 0000246444 00000 n 0000246616 00000 n 0000246788 00000 n 0000246960 00000 n 0000247132 00000 n 0000247304 00000 n 0000247476 00000 n 0000247613 00000 n 0000247785 00000 n 0000247957 00000 n 0000248123 00000 n 0000248291 00000 n 0000248432 00000 n 0000248573 00000 n 0000248714 00000 n 0000248886 00000 n 0000249027 00000 n 0000249164 00000 n 0000249301 00000 n 0000249442 00000 n 0000249579 00000 n 0000249720 00000 n 0000249861 00000 n 0000250002 00000 n 0000250139 00000 n 0000250276 00000 n 0000250448 00000 n 0000250589 00000 n 0000250730 00000 n 0000250867 00000 n 0000251004 00000 n 0000251145 00000 n 0000251311 00000 n 0000251480 00000 n 0000251649 00000 n 0000251786 00000 n 0000251927 00000 n 0000252064 00000 n 0000252201 00000 n 0000252369 00000 n 0000252506 00000 n 0000252675 00000 n 0000252844 00000 n 0000252981 00000 n 0000253118 00000 n 0000253255 00000 n 0000253392 00000 n 0000253533 00000 n 0000253670 00000 n 0000253807 00000 n 0000253948 00000 n 0000254089 00000 n 0000254226 00000 n 0000254363 00000 n 0000254500 00000 n 0000254637 00000 n 0000254778 00000 n 0000254915 00000 n 0000255056 00000 n 0000255197 00000 n 0000255334 00000 n 0000255471 00000 n 0000255608 00000 n 0000255774 00000 n 0000255911 00000 n 0000256048 00000 n 0000256185 00000 n 0000256351 00000 n 0000256488 00000 n 0000256625 00000 n 0000256762 00000 n 0000256899 00000 n 0000257040 00000 n 0000257177 00000 n 0000257314 00000 n 0000257455 00000 n 0000257596 00000 n 0000257737 00000 n 0000257874 00000 n 0000258040 00000 n 0000258177 00000 n 0000258314 00000 n 0000258451 00000 n 0000258588 00000 n 0000258729 00000 n 0000258870 00000 n 0000259007 00000 n 0000259144 00000 n 0000259285 00000 n 0000259422 00000 n 0000259559 00000 n 0000259696 00000 n 0000259833 00000 n 0000259970 00000 n 0000260107 00000 n 0000260244 00000 n 0000260381 00000 n 0000260518 00000 n 0000260655 00000 n 0000260792 00000 n 0000260929 00000 n 0000261097 00000 n 0000261234 00000 n 0000261375 00000 n 0000261512 00000 n 0000261653 00000 n 0000261790 00000 n 0000261927 00000 n 0000262068 00000 n 0000262205 00000 n 0000262342 00000 n 0000262483 00000 n 0000262620 00000 n 0000262757 00000 n 0000262894 00000 n 0000263031 00000 n 0000263172 00000 n 0000263309 00000 n 0000263450 00000 n 0000263591 00000 n 0000263732 00000 n 0000263873 00000 n 0000264014 00000 n 0000264151 00000 n 0000264292 00000 n 0000264433 00000 n 0000265158 00000 n 0000265299 00000 n 0000265440 00000 n 0000266165 00000 n 0000266306 00000 n 0000266447 00000 n 0000267172 00000 n 0000267313 00000 n 0000268038 00000 n 0000268179 00000 n 0000268904 00000 n 0000269045 00000 n 0000269186 00000 n 0000269327 00000 n 0000270048 00000 n 0000270189 00000 n 0000270330 00000 n 0000271051 00000 n 0000271772 00000 n 0000271909 00000 n 0000272046 00000 n 0000272183 00000 n 0000272904 00000 n 0000273625 00000 n 0000274346 00000 n 0000275067 00000 n 0000275788 00000 n 0000276509 00000 n 0000276646 00000 n 0000277367 00000 n 0000278088 00000 n 0000278225 00000 n 0000278362 00000 n 0000279083 00000 n 0000279224 00000 n 0000279365 00000 n 0000279506 00000 n 0000280231 00000 n 0000280372 00000 n 0000280509 00000 n 0000280650 00000 n 0000280791 00000 n 0000280928 00000 n 0000281065 00000 n 0000281233 00000 n 0000281370 00000 n 0000281511 00000 n 0000281648 00000 n 0000281785 00000 n 0000281926 00000 n 0000282063 00000 n 0000282200 00000 n 0000282341 00000 n 0000282478 00000 n 0000282615 00000 n 0000282756 00000 n 0000282897 00000 n 0000283034 00000 n 0000283175 00000 n 0000283316 00000 n 0000283453 00000 n 0000283590 00000 n 0000283731 00000 n 0000283872 00000 n 0000284009 00000 n 0000284146 00000 n 0000284287 00000 n 0000284424 00000 n 0000284561 00000 n 0000284702 00000 n 0000284843 00000 n 0000284980 00000 n 0000285121 00000 n 0000285258 00000 n 0000285399 00000 n 0000285540 00000 n 0000285677 00000 n 0000285818 00000 n 0000285959 00000 n 0000286096 00000 n 0000286237 00000 n 0000286374 00000 n 0000286515 00000 n 0000286656 00000 n 0000286797 00000 n 0000286938 00000 n 0000287075 00000 n 0000287216 00000 n 0000287353 00000 n 0000287490 00000 n 0000287631 00000 n 0000287772 00000 n 0000287913 00000 n 0000288050 00000 n 0000288187 00000 n 0000288328 00000 n 0000288469 00000 n 0000288606 00000 n 0000288747 00000 n 0000288884 00000 n 0000289021 00000 n 0000289158 00000 n 0000289295 00000 n 0000289432 00000 n 0000289569 00000 n 0000289706 00000 n 0000289847 00000 n 0000289984 00000 n 0000290121 00000 n 0000290262 00000 n 0000290403 00000 n 0000290544 00000 n 0000290681 00000 n 0000290818 00000 n 0000290959 00000 n 0000291100 00000 n 0000291237 00000 n 0000291374 00000 n 0000291511 00000 n 0000291652 00000 n 0000291789 00000 n 0000291926 00000 n 0000292067 00000 n 0000292204 00000 n 0000292341 00000 n 0000292482 00000 n 0000292619 00000 n 0000292756 00000 n 0000292897 00000 n 0000293034 00000 n 0000293175 00000 n 0000293316 00000 n 0000293457 00000 n 0000293598 00000 n 0000293739 00000 n 0000293876 00000 n 0000294013 00000 n 0000294154 00000 n 0000294295 00000 n 0000294436 00000 n 0000294573 00000 n 0000294710 00000 n 0000294851 00000 n 0000294988 00000 n 0000295125 00000 n 0000295266 00000 n 0000295403 00000 n 0000295540 00000 n 0000295677 00000 n 0000295818 00000 n 0000295959 00000 n 0000296096 00000 n 0000296237 00000 n 0000296374 00000 n 0000296515 00000 n 0000296652 00000 n 0000296793 00000 n 0000296934 00000 n 0000297071 00000 n 0000297208 00000 n 0000297349 00000 n 0000297486 00000 n 0000297623 00000 n 0000297764 00000 n 0000297901 00000 n 0000298042 00000 n 0000298179 00000 n 0000298348 00000 n 0000298485 00000 n 0000298654 00000 n 0000298823 00000 n 0000298992 00000 n 0000299158 00000 n 0000299330 00000 n 0000299502 00000 n 0000299639 00000 n 0000299811 00000 n 0000299952 00000 n 0000300124 00000 n 0000300261 00000 n 0000300402 00000 n 0000300539 00000 n 0000300680 00000 n 0000300817 00000 n 0000300958 00000 n 0000301095 00000 n 0000301236 00000 n 0000301373 00000 n 0000301514 00000 n 0000301651 00000 n 0000301788 00000 n 0000301929 00000 n 0000302066 00000 n 0000302207 00000 n 0000302348 00000 n 0000302485 00000 n 0000302655 00000 n 0000302825 00000 n 0000302966 00000 n 0000303135 00000 n 0000303276 00000 n 0000303445 00000 n 0000303586 00000 n 0000303727 00000 n 0000303864 00000 n 0000304001 00000 n 0000304138 00000 n 0000304275 00000 n 0000304416 00000 n 0000304557 00000 n 0000304698 00000 n 0000304839 00000 n 0000304980 00000 n 0000305121 00000 n 0000305262 00000 n 0000305403 00000 n 0000305544 00000 n 0000305685 00000 n 0000305826 00000 n 0000305967 00000 n 0000306108 00000 n 0000306249 00000 n 0000306390 00000 n 0000306531 00000 n 0000306672 00000 n 0000306841 00000 n 0000306982 00000 n 0000307707 00000 n 0000308432 00000 n 0000309157 00000 n 0000309326 00000 n 0000310057 00000 n 0000310788 00000 n 0000311519 00000 n 0000311688 00000 n 0000311825 00000 n 0000311962 00000 n 0000312099 00000 n 0000312236 00000 n 0000312373 00000 n 0000312510 00000 n 0000313241 00000 n 0000313382 00000 n 0000313519 00000 n 0000313660 00000 n 0000313797 00000 n 0000313938 00000 n 0000314079 00000 n 0000314220 00000 n 0000314357 00000 n 0000314527 00000 n 0000314664 00000 n 0000314801 00000 n 0000314938 00000 n 0000315110 00000 n 0000315247 00000 n 0000315384 00000 n 0000315521 00000 n 0000315658 00000 n 0000315799 00000 n 0000315936 00000 n 0000316077 00000 n 0000316214 00000 n 0000316351 00000 n 0000316488 00000 n 0000316629 00000 n 0000316766 00000 n 0000316903 00000 n 0000317040 00000 n 0000317181 00000 n 0000317318 00000 n 0000317455 00000 n 0000317592 00000 n 0000317729 00000 n 0000317870 00000 n 0000318007 00000 n 0000318144 00000 n 0000318281 00000 n 0000318418 00000 n 0000318555 00000 n 0000318692 00000 n 0000318829 00000 n 0000319001 00000 n 0000319138 00000 n 0000319275 00000 n 0000319416 00000 n 0000319553 00000 n 0000319725 00000 n 0000319862 00000 n 0000319999 00000 n 0000320140 00000 n 0000320312 00000 n 0000320453 00000 n 0000320594 00000 n 0000320766 00000 n 0000320907 00000 n 0000321044 00000 n 0000321216 00000 n 0000321388 00000 n 0000321525 00000 n 0000321666 00000 n 0000321838 00000 n 0000321979 00000 n 0000322120 00000 n 0000322261 00000 n 0000322402 00000 n 0000322543 00000 n 0000322684 00000 n 0000322821 00000 n 0000322958 00000 n 0000323099 00000 n 0000323236 00000 n 0000323373 00000 n 0000323514 00000 n 0000323651 00000 n 0000323792 00000 n 0000323929 00000 n 0000324066 00000 n 0000324203 00000 n 0000324340 00000 n 0000324477 00000 n 0000324614 00000 n 0000324755 00000 n 0000324892 00000 n 0000325029 00000 n 0000325170 00000 n 0000325307 00000 n 0000325448 00000 n 0000325585 00000 n 0000325722 00000 n 0000325859 00000 n 0000325996 00000 n 0000326133 00000 n 0000326270 00000 n 0000326407 00000 n 0000326548 00000 n 0000326685 00000 n 0000326822 00000 n 0000326963 00000 n 0000327100 00000 n 0000327237 00000 n 0000327378 00000 n 0000327519 00000 n 0000327656 00000 n 0000327797 00000 n 0000327938 00000 n 0000328075 00000 n 0000328212 00000 n 0000328353 00000 n 0000328490 00000 n 0000328631 00000 n 0000328768 00000 n 0000328909 00000 n 0000329081 00000 n 0000329222 00000 n 0000329394 00000 n 0000329566 00000 n 0000329738 00000 n 0000329910 00000 n 0000330082 00000 n 0000330254 00000 n 0000330426 00000 n 0000330598 00000 n 0000330770 00000 n 0000330942 00000 n 0000331114 00000 n 0000331286 00000 n 0000331458 00000 n 0000331630 00000 n 0000331803 00000 n 0000331976 00000 n 0000332149 00000 n прицеп ] >> startxref 0 %% EOF 27 0 объект> поток «Y Ѹ 6Wщ_xq * MvsiKzJC S2BZ ߋ Ԭ «hJiS0u7xGB; ertw | OI #] KJtCΙяqCBgqsz / ^ е ; WncY ގ5 {> I` {, е U, «* СОО (zoG_f} JE-г \ KVPҸ [4HM: NCoo7hB * 3 / E8n-Д `PTC-5 (JNP {SJaH Hl2k.d-2_ * дt ש v64Zr, D ߃ ж «-F |! \ OOfWqәUa с
.- Эта статья о железе и металле. Для инструмента под названием железо, см. Глажение.

Железо является химическим элементом и металлом. Это самый распространенный химический элемент на Земле (по массе) и наиболее широко используемый металл. Он составляет большую часть ядра Земли и является четвертым наиболее распространенным элементом в земной коре.
Металл много используется, потому что он прочный и дешевый.Железо является основным ингредиентом, используемым для производства стали. Сырое железо является магнитным (притягивается к магнитам), а его сложный магнетит является постоянно магнитным.
В некоторых регионах железо использовалось около 1200 г. до н.э. Это событие считается переходом от бронзового века к железному веку.
Физические свойства [изменить | изменить источник]
Железо — серый, серебристый металл. Он магнитный, хотя разные аллотропы железа имеют разные магнитные свойства. Железо легко найти, добыть и выплавить, поэтому оно так полезно.Чистое железо мягкое и очень податливое.
Химические свойства [изменить | изменить источник]
Железо реагирует. Реагирует с большинством кислот, таких как серная кислота. При взаимодействии с серной кислотой образуется сульфат железа. Эта реакция с серной кислотой используется для очистки металла.
Железо реагирует с воздухом и водой с образованием ржавчины. Когда ржавчина отслаивается, подвергается большему воздействию железа, что позволяет большему количеству железа ржаветь. В конце концов, весь кусок железа заржавел. Другие металлы, такие как алюминий, не ржавеют.Железо может быть сплавлено с хромом, чтобы сделать нержавеющую сталь, которая не ржавеет в большинстве условий.
Железный порошок может реагировать с серой с образованием сульфида железа (II), твердого твердого вещества черного цвета. Железо также реагирует с галогенами с образованием галогенидов железа (III), таких как хлорид железа (III). Железо реагирует с галогенводородными кислотами с образованием галогенидов железа (II), таких как хлорид железа (II).
Химические соединения [изменить | изменить источник]
Железо образует химические соединения с другими элементами. Обычно другой элемент окисляет железо.Иногда берут два электрона, а иногда три. Соединения, в которых в железе содержится два электрона, называются соединениями железа. Соединения, в которых в железе содержится три электрона, называются соединениями железа. Соединения железа содержат железо в степени окисления +2. Соединения железа содержат железо в степени окисления +3. Соединения железа могут быть черного, коричневого, желтого, зеленого или фиолетового цвета.
Соединения железа являются слабыми восстановителями. Многие из них зеленые или синие. Наиболее распространенным соединением железа является сульфат железа.
Соединения железа являются окислителями. Многие из них коричневые. Наиболее распространенным соединением железа является оксид железа, то же самое, что ржавчина. Одна из причин, по которой железо ржавеет, заключается в том, что оксид железа является окислителем. Он окисляет железо, ржавеет даже под краской. Вот почему, если на краске есть небольшая царапина, все это может ржаветь.
Соединения железа (II) [изменить | изменить источник]
Соединения в степени окисления +2 являются слабыми восстановителями. Они обычно светлые.Они реагируют с кислородом в воздухе. Они также известны как соединения железа.
- Сульфид железа (II), блестящий химикат, который реагирует с кислотами с выделением сероводорода, найденный в земле
- Сульфат железа (II), сине-зеленый кристаллический химикат, полученный путем взаимодействия серной кислоты со сталью, используемый для уменьшения ядов, таких как хромат в бетоне
- Хлорид железа (II), бледно-зеленый кристаллический химикат, полученный взаимодействием соляной кислоты со сталью
- Гидроксид железа (II), темно-зеленый порошок, полученный путем электролиза воды с железным анодом, реагирует с кислородом и становится коричневым
- Оксид железа (II), черный, легковоспламеняющийся, редкий
Состояние смешанного окисления [изменить | изменить источник]
Эти соединения редки; только один распространен.Они найдены в земле.
Соединения железа (III) [изменить | изменить источник]
Соединения в степени окисления +3 обычно коричневые. Они являются окислителями. Они едкие. Они также известны как соединения железа.
- Оксид железа (III), ржавчина, красно-коричневый, растворяется в кислоте
- Хлорид железа (III), ядовитый и едкий, растворяется в воде с образованием темно-коричневого кислого раствора. Изготовлен путем взаимодействия железа с соляной кислотой и окислителем
- Нитрат железа (III), светло-фиолетовый, едкий, используется при травлении
- Сульфат железа (III), редкий, светло-коричневый, растворяется в воде.Изготовлен путем взаимодействия железа с серной кислотой и окислителем.
Во вселенной много железа, потому что это конечная точка ядерных реакций в больших звездах. Это последний элемент, который будет произведен до того, как сильный коллапс сверхновой рассеет железо в космосе.
Металл является основным ингредиентом в ядре Земли. Рядом с поверхностью он находится в виде соединения железа или железа. Некоторые метеориты содержат железо в виде редких минералов. Обычно железо находится в виде гематитовой руды в земле, большая часть которой была получена во время Великого оксигенационного события.Железо можно извлечь из руды в доменной печи. Некоторое количество железа находится в виде магнетита.
В мясе есть соединения железа. Железо является важной частью гемоглобина в эритроцитах.

Чугун производится на крупных заводах, называемых , , путем восстановления гематита углеродом (кокс). Это происходит в больших контейнерах, называемых доменными печами. Доменная печь заполнена железной рудой, коксом и известняком. Вдыхается очень горячий поток воздуха, в результате чего происходит горение кокса.Сильная жара заставляет углерод реагировать с железной рудой, отбирая кислород у оксидов железа и выделяя углекислый газ. Углекислый газ является газом, и он покидает смесь. В железе есть немного песка. Известняк, который сделан из карбоната кальция, превращается в оксид кальция и углекислый газ, когда известняк очень горячий. Оксид кальция вступает в реакцию с песком, образуя жидкость, называемую шлаком. Шлак сливается, оставляя только железо. Реакция оставит чистое жидкое железо в доменной печи, где это может быть сформировано и укреплено после охлаждения.Почти все металлургические заводы сегодня являются частью сталелитейных заводов, и почти все железо превращается в сталь.
Есть много способов работы железа. Железо можно закалить, нагревая кусок металла и брызгая его в холодную воду. Это может быть смягчено, нагревая это и позволяя этому медленно остывать. Это может также быть отпечатано тяжелым прессом. Его можно втянуть в провода. Это может быть свернуто, чтобы сделать листовой металл.
В Соединенных Штатах большая часть железа была взята с земли в Миннесоте, а затем отправлена на корабле в Индиану и Мичиган, где она была превращена в сталь.
Как металл [изменить | изменить источник]

Железо используется больше, чем любой другой металл. Это сильно и дешево. Он используется для изготовления зданий, мостов, гвоздей, винтов, труб, балок и башен.
Железо не очень реактивно, поэтому его легко и дешево извлечь из руды. Он очень прочный после изготовления из стали и используется для армирования бетона.
Существуют разные виды железа. Чугун — это железо, изготовленное способом, описанным выше в статье.Это трудно и хрупко. Он используется для изготовления таких вещей, как крышки ливневых канализаций, крышки люков и блоки двигателей (основная часть двигателя).
Сталь — самая распространенная форма железа. Стали бывают разных форм. Мягкая сталь — это сталь с низким процентным содержанием углерода. Он мягкий и легко сгибается, но не трескается легко. Используется для гвоздей и проводов. Углеродистая сталь тверже, но более хрупкая. Используется в инструментах.
Существуют и другие виды стали. Нержавеющая сталь из-за содержания хрома устойчива к ржавчине, а никель-железные сплавы могут оставаться прочными при высоких температурах.Другие стали могут быть очень твердыми, в зависимости от добавленных сплавов.
Кованое железо легко формируется и используется для изготовления заборов и цепей.
Очень чистое железо мягкое и может легко ржаветь (окисляться). Это также довольно реактивный.
В качестве соединения [изменить | изменить источник]
Соединения железа используются для нескольких целей. Хлорид железа (II) используется для очистки воды. Хлорид железа (III) также используется. Сульфат железа (II) используется для восстановления хроматов в цементе. Некоторые соединения железа используются в витаминах.
Дефицит железа — самый распространенный недостаток питания в мире. [1] [2] [3]
Наше тело нуждается в железе, чтобы помочь кислороду проникнуть в наши мышцы, потому что он лежит в основе некоторых важных макромолекул в нашем организме, таких как гемоглобин, которые заставляют его работать лучше. Многие злаки содержат некоторое количество железа (элемент , металл , железо). [4] [5] Добавляется в злаки в виде крошечных металлических опилок. Иногда можно увидеть осколки, взяв чрезвычайно сильный магнит и положив его в коробку.Магнит притянет эти железки. Употребление этой маленькой металлической стружки не вредно для нашего организма. [6]
Железо является наиболее доступным для организма при добавлении к аминокислотам — железо в этой форме усваивается в десять-пятнадцать раз больше, чем элемент. [7] Железо также содержится в мясе, например, в стейке. Железо, обеспечиваемое диетическими добавками, находится в форме химического вещества, такого как сульфат железа (II), который дешев и хорошо усваивается. Тело не будет потреблять больше железа, чем нужно, и обычно ему нужно очень мало.Железо в красных кровяных клетках перерабатывается системой, которая разрушает старые клетки. Потеря крови из-за травмы или паразитной инфекции может быть более серьезной. [8]
Железо токсично, когда в организм поступает большое количество. Когда принимается слишком много таблеток железа, люди (особенно дети) заболевают. Кроме того, существует генетическое заболевание, которое нарушает регуляцию уровня железа в организме.
Существуют химические вещества, которые связываются с железом, что врачи могут назначить.
- 01 Центры по контролю и профилактике заболеваний (2002).«Дефицит железа — США, 1999–2000». MMWR . 51 : 897–9.
- 01 Hider, Robert C .; Kong, Xiaole (2013). «Глава 8. Железо: влияние перегрузки и дефицита». В Астрид Сигел, Хельмут Сигел и Роланд К. О. Сигел (ред.). Взаимосвязь между ионами основных металлов и человеческих заболеваний . Металлические ионы в науках о жизни. 13 . Springer. стр. 229-294. DOI: 10.1007 / 978-94-007-7500-8_8.
- — Длухи, Адриенн С.; Outten, Caryn E. (2013). «Глава 8.4 Поглощение, оборот и хранение железа». В Банчи, Люсия (ред.) (Ред.). Металломика и ячейка . Металлические ионы в науках о жизни. 12 . Springer. DOI: 10.1007 / 978-94-007-5561-1_8. ISBN 978-94-007-5560-4 . CS1 maint: дополнительный текст: список редакторов (ссылка) электронная книга ISBN 978-94-007-5561-1 ISSN 1559-0836 электронная ISSN 1868-0402
- № «Испытание стойкости железа в злаках». Министерство сельского хозяйства США.Получено 2010-01-29.
- ↑ Адамс, Сесил. Возвращение прямого допинга . Нью-Йорк: Баллантайн Букс, 1994
- ↑ Фелтон, Брюс. Один из видов . Нью-Йорк: Уильям Морроу и Ко, 1992
- — Пинеда О, Ашмид Х.Д. (2001). «Эффективность лечения железодефицитной анемии у детей грудного и раннего возраста с помощью бис-глицинатного хелата железа». Питание . 17 (5): 381–4. DOI: 10.1016 / S0899-9007 (01) 00519-6. PMID 11377130.
- ↑ Andrews N.C. 2000. Нарушения обмена железа. Медицинский журнал Новой Англии . Соответствующая корреспонденция, опубликованная в NEJM 342 : 1293-1294.
Оксид железа 5 | Воздушные окна
TL; DW: Старая школа, сильно окрашенная эмуляция ленты Airwindows.
IronOxide5
(доступна сборка начальной версии: IronOxideInitial5 является первой версией до того, как я добавил контроль уровня шума. Я предоставляю его на случай, если людям это нужно в особых обстоятельствах, но вы НЕ должны его иметь и полная версия Iron Oxide 5, установленная одновременно, потому что они имеют идентификаторы плагинов, и вы запутаете свой компьютер)
Наследие этого плагина уходит в прошлое.Много лет назад я кодировал некоторые из моих первых плагинов AU, и у некоторых моих друзей был неудачный опыт с компанией, которая продала самый большой плагин эмуляции ленты того времени. Возмущенный, я напал на драку: я запишу для них замену, которая будет делать то же самое, звучит лучше и продается за 60 долларов (позже 50 долларов). И это был оксид железа. У него был один элемент управления «ips», привод и выходной уровень.
Затем я остановился на этом с оксидом железа 2. Этот разделил верхнюю и нижнюю обрезки «ips», чтобы вы могли изменить качество «bandpassy».Он использовал тот же необычный алгоритм, но сделал его более гибким. Он также включал в себя необычный вид сглаживания в виде «шума ленты», который размыл поворот.
Оксид железа 3 добавлен флаттер. В этот момент мы отошли от строго нулевой задержки: вместо этого плагин объявляет нулевую задержку, но производит размытое размытие по одному или двум сэмплам, диапазон, который охватывает флаттер. Это сохраняется для оксида железа 4 и 5, и именно так работает текущий свободный VST оксид железа.
Оксид железа 4 добавил еще кое-что, что (узнайте) также присутствует в Delta Labs Effectron: контроль inv / dry / wet.Это сохраняется при использовании оксида железа 5. Как вы его используете, настройте тон оксида железа, который подчеркивает частотный диапазон (например, средние частоты). Ведите его или оставьте его в чистоте… но начните устанавливать регулятор в положение inv (перевернутое положение). Вы вычтете его из сухого, вызывая провал, а не повышение, но если вы насыщаете «ленту», то провал оставит динамическую энергию в области, подлежащей отмене: он будет вырезать жир, оставляя удар. Перегружайте секцию «ленты» сильнее (и убирайте «инв»), чтобы получить больше ударов, или оставьте ее чистой и используйте ее только для того, чтобы отменить область.Это необычный эффект, но он работает.
Iron Oxide 5 — это все, плюс уроки из серии плагинов «Purest» (в основном все еще в очереди, чтобы быть выпущенными позже), чтобы произвести то же самое, что и Iron Oxide 4, но еще более чистый, резонансный и интенсивный. На самом деле ни один из них не является плагином типа «смешанный бизнес» (хотя я не являюсь вашим боссом): он слишком сильно окрашен и искажен. Они больше о том, как «заставить эту ловушку действительно лаять» и так далее. Хотя, конечно, поскольку я не являюсь вашим боссом, я не могу помешать вам использовать его в полной смеси.Все, что я могу сделать, это сказать, что ToTape идет, и это СОВРЕМЕННАЯ эмуляция ленты. Это старая школа, шумная, очевидная эмуляция ленты, полная гранжа и лая 🙂
И это бесплатно, потому что поддерживается Patreon. Мы преодолели порог, когда я выпускаю плагины «лучших хитов» бывшей Kagi, и пока я остаюсь более 600 долларов в месяц, это продолжается. Если я получу больше 800 долларов, я тоже начну использовать открытый плагин, и если я получу больше 1000 долларов в месяц, я буду выпускать два из этих лучших хитов в месяц, в дополнение к другим плагинам и соответствующим плагинам и видео на YouTube, показывающим, как это сделать.
Великолепное время гарантировано для всех, и я надеюсь, что вам понравится оксид железа 5. Оставайтесь с нами для «TapeDust», аспекта «аналогового зернистости ленты» оксида железа, изолированного и поставленного под ваш контроль, чтобы вы могли отделить его от полного плагин (то есть без перегрузки или искажения), и я открыт для создания «Классического оксида железа», который восходит к Версии 1 и действует как гораздо более простая искаженная эмуляция bandpassy, где все это началось. Просите, и вы получите 🙂
,